BRAF突变型结直肠癌(CRC)患者预后较差,现有治疗手段在这一突变患者群体中的疗效不尽理想。对于BRAF突变CRC,适当的检查和治疗在临床上是一项较大的挑战,包括发病机制,转移通路和新治疗靶点,都需要更多研究。
在过去几十年,肿瘤靶向治疗领域发生了翻天覆地的变化,但是,BRAF这一靶点的突破都在其他瘤种中,比如黑色素瘤,结直肠癌鲜有进展。
本文简要回顾一下BRAF突变型CRC。
BRAF突变在所有肿瘤中的突变率在7%左右,但是不同癌症之间差别很大。黑色素瘤BRAF突变率接近50%,而结直肠癌为10-25%。
MAPK信号通路
2002年,Nature杂志发表了题为《Mutations of the BRAF gene in human cancer》的文章,首次阐述了癌基因BRAF突变。研究者在癌症基因组计划中发现66%的黑色素瘤细胞系内存在BRAF激酶结构域异常。自那时起,已经发现了超过100种BRAF基因突变。最常见的是V600E突变:BRAF基因外显子15的第1799位核苷酸T突变为A,导致其编码的缬氨酸被谷氨酸取代。
BRAF是RAF三个亚型之一,是MAPK通路重要的转导因子。BRAF-V600E突变体模拟了野生BRAF S598/T601的磷酸化,持续和最大限度的异常增强了激酶活性。
促分裂素原活化蛋白激酶(MAPK)信号转导通路是细胞内最重要的信号通路之一,MAPK/ERK途径主要由RAS→RAF→MEK→ERK等蛋白激酶组成,通过依次催化下级蛋白激酶发生磷酸化而激活整个信号通路,活化的ERK可以通过影响细胞周期MITF等因子促使细胞生长过度,导致正常细胞向肿瘤细胞转化。
MAPK/ERK通路简要图如下所示:
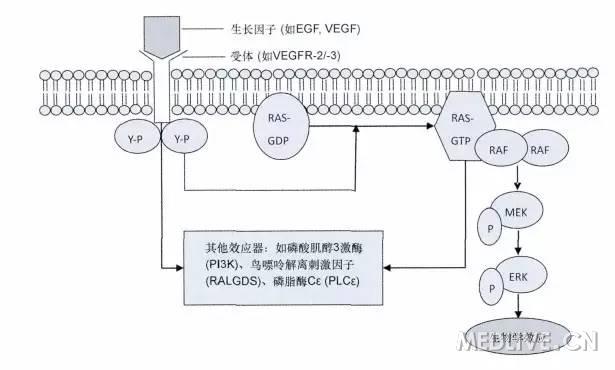
BRAF突变的检测和筛查
BRAF突变种类众多,但临床上针对CRC的主要检测目标还是V600E突变。随着二代测序(NGS)技术的不断应用,检测非V600E突变也越来越容易。比如,梅奥诊所的一例转移性CRC患者,NGS检测发现BRAF存在20%的非V600E突变。但是,这些非V600E突变在实验研究中作用不尽相同:激活激酶活性,无活性,抑制激酶活性均存在。
截至目前,仅有一项研究报道了非V600E突变患者的临床结局,该研究在10例CRC患者中检测到594个外显子的596个突变。与V600突变患者相比,非V600E突变患者的分子特征、病理参数、临床结局均有较大差异。
临床特点与预后
与无突变的结直肠癌相比,BRAF突变型CRC患者的年龄偏大,女性居多,微卫星不稳定可能性大、组织级别高,淋巴结转移率和局部晚期发生率高。该型患者的原发灶多位于近端结肠(右半),容易较早出现腹膜和远处淋巴结转移。
在预后方面,无论是早期还是晚期转移CRC,BRAF突变状态都是较强的生存预测因素。术后辅助治疗后,BRAF突变型CRC的无病生存期更短,复发后的总生存期更差。PETACC-3研究检测了1404例Ⅱ-Ⅲ期结肠癌患者的BRAF和KRAS突变,结果显示,BRAF突变型患者的总生存劣于野生型患者。当根据微卫星不稳定分层后,这种差异更加明显。
对于肝脏寡转移,在转移灶根治性切除后,与野生型患者相比,BRAF突变型的无复发生存时间<6个月,且总生存较差。若肝转移无法切除则预后更差。从整体来看,标准细胞毒化疗后,BRAF突变CRC患者的中位生存期只有野生型患者的1/2-1/3。
BRAF突变状态也可作为EGFR抑制剂治疗的预测指标,突变型患者治疗反应较差。
2014年NEJM的一项研究显示,较强的化疗方案FOLFOXIRI联合贝伐珠单抗可能是BRAF突变型CRC的治疗选择之一。与FOLFIRI方案相比,FOLFOXIRI+贝伐珠单抗使转移性CRC患者的PFS延长了2.5个月。但是,即使是很强的化疗,BRAF突变型CRC患者的生存期依然远远落后于野生型患者,中位OS分别为19.0个月vs 41.7个月。
靶向治疗
由于细胞毒药物的获益有限,加之黑色素瘤中针对BRAF突变的靶向治疗前景良好,越来越多的临床试验将BRAF作为一个重要的目标驱动基因。
其中最尴尬的是选择性BRAF-V600E抑制剂vemurafenib单药治疗21例CRC,结果很不理想:1例患者达到部分缓解,总缓解率只有可怜的5%,而该药在黑色素瘤中总缓解率可有60-75%。
失败不可怕,单药vemurafenib的经验告诉我们:
►1.BRAF-V600E单一突变难以成就靶向治疗;
►2.同一种突变,在结直肠癌和黑色素瘤中有完全不同的疗效反应,说明其内在机制的复杂。
事实上,在CRC和黑色素瘤细胞系内加入BRAF抑制剂,两者的下游信号ERK磷酸化(pERK)的水平明显不同,CRC细胞系pERK非常高,提示上游MAPK通路抑制不足。
另一种靶向治疗策略是BRAF抑制剂(dabrafenib)联合MEK抑制剂(trametinib)。在纳入43名转移性BRAF突变型CRC患者的研究中,4例(9%)达到部分缓解,1例(2%)达到持续的完全缓解。当然,这样的成绩远不能让人觉得欣慰,但从中我们可以吸取经验:
►1.唯一出现完全缓解的患者并没有接受系统治疗,这可能是巧合,但也不能完全排除细胞毒药物对BRAF抑制剂的作用环境产生了影响。
►2.从9例患者治疗后15天的活检组织分析来看,pERK水平是有所下降,但下降程度远不及黑色素瘤(37% vs 84%)。
该研究虽然提供了联合靶向的临床有效性数据,但也说明阻断CRC的MAPK通路着实是道难题。
2012年,Nature杂志发文揭示了CRC对BRAF抑制剂抵抗的可能机制,当CRC细胞暴露于BRAF抑制剂时,EGFR异常激活增加,从而绕过MAPK,导致PI3K和AKT通路信号加强。当EGFR抑制剂与BRAF抑制剂合用时,MEK、ERF、AKT相关通路信号转导都受到抑制。这些研究结果催生了众多联合用药试验,如下图:
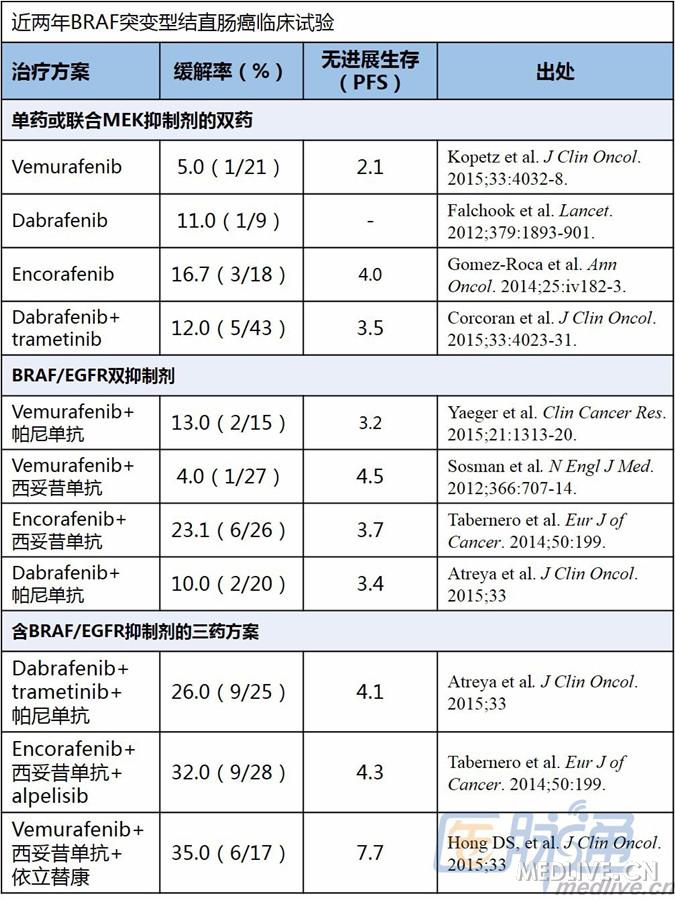
如上图所示,EGFR抑制剂联合BRAF抑制剂的研究还在摸索中,尽管缓解率和PFS都不理想,但鉴于双抑制剂提供的持续性渐进式改善,未来或可成为一种治疗策略。
在EGFR/BRAF双抑制剂的基础上增加第三种药物值得关注。
◆第一种联合是dabrafenib(BRAF抑制剂)+帕尼单抗(EGFR抑制剂)+ trametinib(MEK抑制剂);从最后一次数据更新来看,35名患者中9例(26%)至少达到部分缓解。
◆第二种联合是encorafenib(BRAF抑制剂)+西妥昔单抗(EGFR抑制剂)+ alpelisib(PI3K抑制剂);2014年的更新数据表明,28名患者中9例(32%)至少达到部分缓解。
◆第三种联合是vemurafenib(BRAF抑制剂)+西妥昔单抗+依立替康;17例转移性CRC患者中6例(35%)至少达到部分缓解。
展望
有关结直肠癌BRAF突变的研究众多,到目前为止,还未转化成为确实的临床获益。从黑色素瘤中引申出的单药BRAF抑制剂治疗,在结直肠癌中以失败告终,折射出我们对信号转导通路理解的浅薄。
挖掘BRAF突变的价值,不仅仅是告诉我们患者预后如何,更为重要的是将其作为治疗靶点改善预后。肿瘤存在星罗棋布的多重耐药机制, 多种手段及联合用药治疗也许能更好地封锁各条必经信号通路。单打独斗不行,联合EFGR、MEK和PI3K激酶抑制剂多管齐下,或许可以有所突破。
另外,BRAF突变型CRC患者微卫星不稳定发生率高,未来甚至可以考虑联合免疫药物PD-1抑制剂增效。
从发现肿瘤基因突变,到研究突变的临床价值,再到开发靶向药物,每一步都需要运气和努力。结直肠癌的靶向治疗步履蹒跚,或许真的需要一点运气。
信源:
1.Jeremy C.et al.Understanding BRAF-Mutant Colorectal Cancer.Am.asco.org.
2.申付文,等. 黑色素瘤小分子靶向药物研究进展[J].中国新药杂志,2015,03:281-287.
(本网站所有的内容,凡注明来源为“医脉通”,版权均归医脉通所有,欢迎转载,但请务必注明出处,否则将追究法律责任。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)
© 国家肿瘤质控中心 版权所有 | www.china-rt.cn 京ICP备12038261号-9
主管: 国家卫生健康委员会 | 协管:中国医学科学院肿瘤医院 | 授权文号:卫医政发[2009]51号
技术支持:北京全域医疗技术集团有限公司 | 电话:400-626-0656